慢性难愈性、烧伤和感染性创面严重影响患者生活,若治疗不及时,可能致残或致死,是亟需解决的临床难题。此类创面常因感染和微环境恶化而难以愈合。水凝胶因能吸收渗液、保持湿润,常用于创面修复,但现有产品多以保护为主,缺乏针对性响应,抗感染和促愈合效果有限。为此,课题组致力于研发兼具抗感染和促愈合功能的微环境调控型水凝胶敷料,并开展了系列研究。
1.壳聚糖/葛根素水凝胶用于感染创面修复
团队基于中药研磨工艺,采用一步研磨法构建具有不同葛根素含量的可注射壳聚糖/葛根素(C@P)自组装纳米纤维水凝胶。研磨过程中引入的机械力可促进壳聚糖和葛根素分子间的有效碰撞,加速分子自组装过程。壳聚糖的氨基在非共价键和亲疏水作用下定向排列,提高了凝胶的Zeta电位,进而赋予凝胶优异的抗菌能力。C@P凝胶通过抗菌和抗炎协同作用,抑制创面细菌增殖,缓解创面炎症,可有效促进感染创面的愈合。(Small, 2022, 18(21), 2201766)
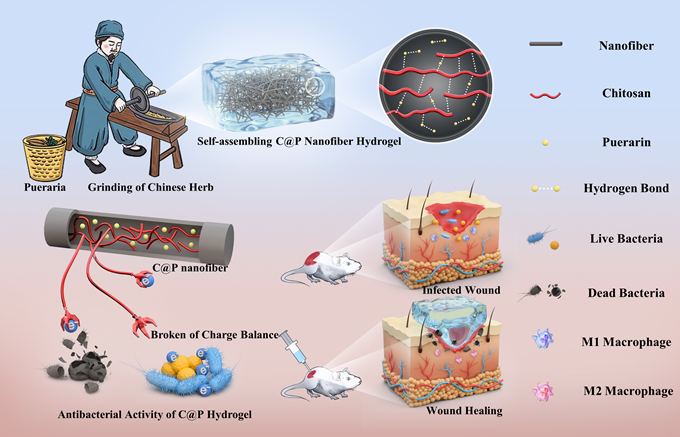
图1. 受中药研磨工艺启发的机械力诱导自组装水凝胶治疗感染创面示意图。
2. β-环糊精复合水凝胶创面修复研究
β-环糊精(β-CD)水凝胶由于其良好的生物相容性、稳定性和可修饰性,被广泛应用于创面修复。然而,缺乏抗菌性能和较差的机械性能限制了其在临床中的进一步应用。团队通过综合改性方法设计并构建β-CD/PEI/PVA(BPP)复合水凝胶,主要探究了不同组分对复合凝胶理化性能和生物学性能的影响规律。BPP中PVA物理交联网络使得材料的可逆变形性得以提高,β-CD/PEI(BP)化学交联网络使得复合水凝胶的储能模量与强度有较大提升。水凝胶具有优异的抗菌性能和生物相容性,其抗菌性能的主要来源是阳离子聚合物PEI经过化学改性制备的叔胺化聚乙烯亚胺TPEI。通过大鼠皮肤全损感染性模型探究了水凝胶组分对创面修复的作用规律,发现BPP水凝胶通过有效杀伤创面处的细菌、减轻由细菌感染导致的炎症、促进胶原有序沉积和VEGF促血管生成因子的表达,加快创面愈合的进程。(Composites Part B: Engineering, 2022, 238:109921)
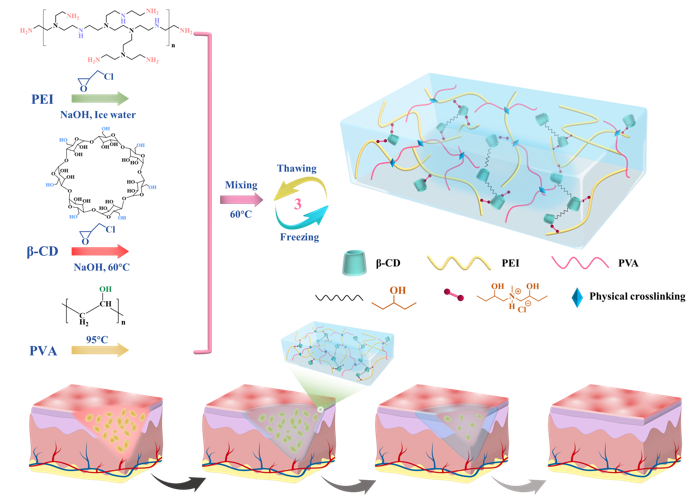
图2.水凝胶成胶过程及其促创面修复示意图。
3.电活性水凝胶用于糖尿病创面修复
皮肤是典型具备电生理特性的组织。电刺激可模拟受损组织周围内源性电场,诱导细胞向损伤部位迁移并调控细胞行为,加速伤口愈合。借助电活性材料响应外场产生电信号,能重建伤口电生理微环境。超声波作为生物医学领域广泛应用的外场刺激,具备优异的组织穿透能力,可用于实现声电转换。基于此,团队设计了一种超声响应复合水凝胶,以明胶/聚乙烯醇(PVA)互穿聚合物网络为基底,掺杂铌酸钾钠压电纳米晶体与还原氧化石墨烯(rGO),通过声电转换促进局部神经血管再生,加速糖尿病伤口愈合(图3,Materials Today, 2025, 84: 48-64)。
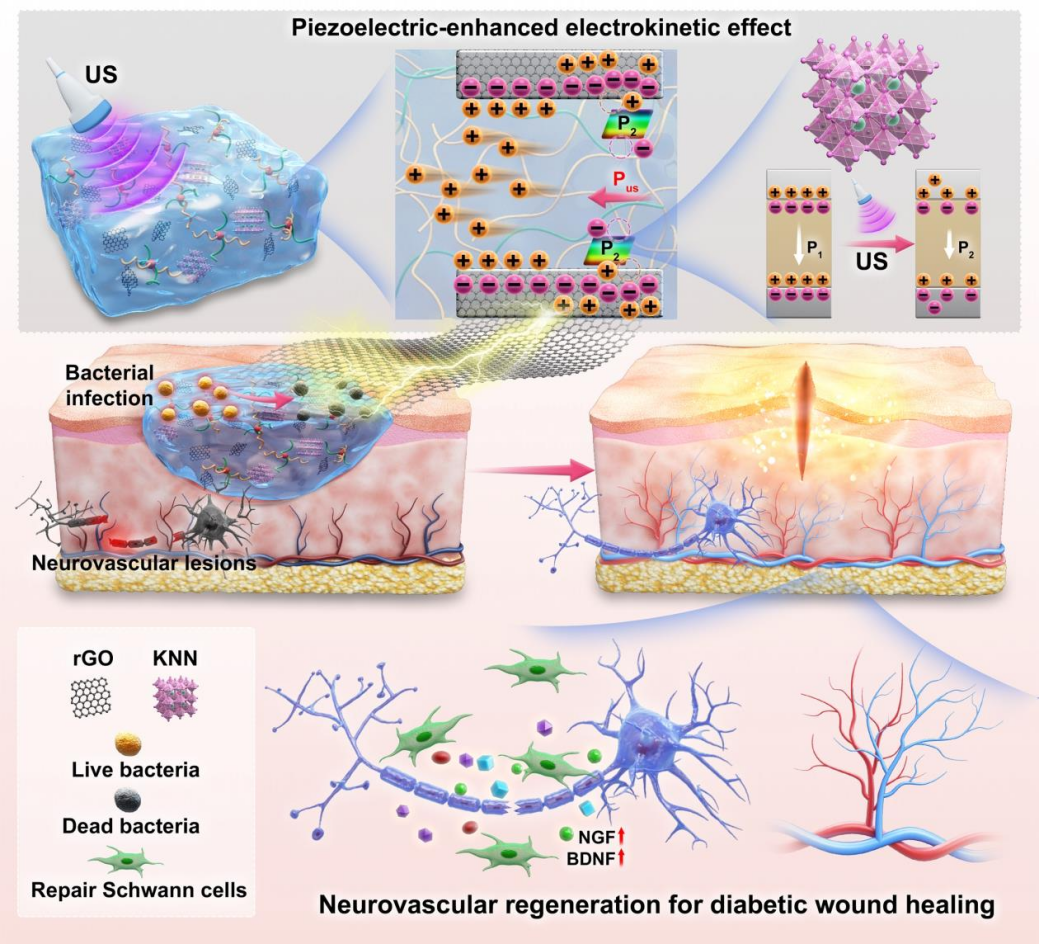
图3.超声响应压电复合水凝胶的声电转换和促进糖尿病创面愈合示意图。
此外,团队构建了一种姜黄素负载的rGO/明胶/PVA复合水凝胶(CGGP),兼具超声响应电刺激与可控药物释放功能(图4)。超声触发双电层离子迁移与rGO-姜黄素间电子转移,增强电信号并调控姜黄素释放。超声响应CGGP水凝胶能调节巨噬细胞向抗炎M2型极化;促进施万细胞神经营养因子的分泌;提高内皮细胞活性并促进血管生成;促进成纤维细胞迁移。动物实验结果显示该水凝胶能够有效促进创面神经再生及血管生成,显著加速糖尿病创面愈合。(Advanced Functional Materials, 2025, https://doi.org/10.1002/adfm.202510243)
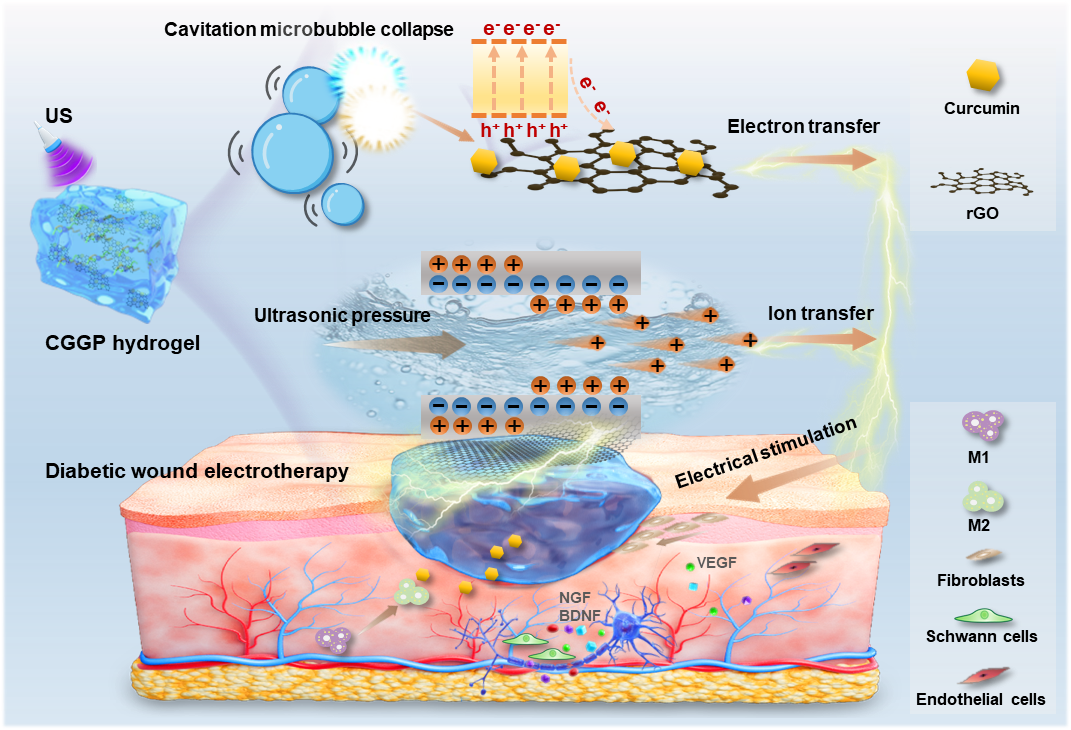
图4.基于界面离子/电子转移的超声响应复合水凝胶用于糖尿病创面修复示意图。
4.抗氧化金属氮碳纳米酶用于炎症创面治疗
炎症创面主要特征是免疫反应失调导致的活性氧(ROS)水平高。碳基纳米酶可模拟天然抗氧化酶催化清除ROS,同时具备优异的结构稳定性,可实现ROS高效、持久清除。针对现有碳基纳米酶制备工艺繁琐且分散性差等问题,团队基于金属-席夫碱配位,开发了一种无热解通用合成策略用于制备可清除ROS的金属氮掺杂碳材料(M-NC)(Carbon, 2023, 201, 439-448)。以Fe-NC为例,详细探讨了其形成过程和类酶活性位点,以及Fe含量对类酶活性的影响规律。该合成策略可扩展至其他过渡金属氮掺杂碳材料(Cu、Mn、Co、Zn和Ni)。在此基础上,引入“惰性-活性金属原子对”调控Fe位点电子结构,制备FeZn-NC双金属氮掺杂碳材料,提出“缺电子效应”增强的CAT-like活性机制,通过ROS清除和免疫调控实现急性炎症创面治疗(图5,Advanced Functional Materials, 2024, 34(52): 2411202)。
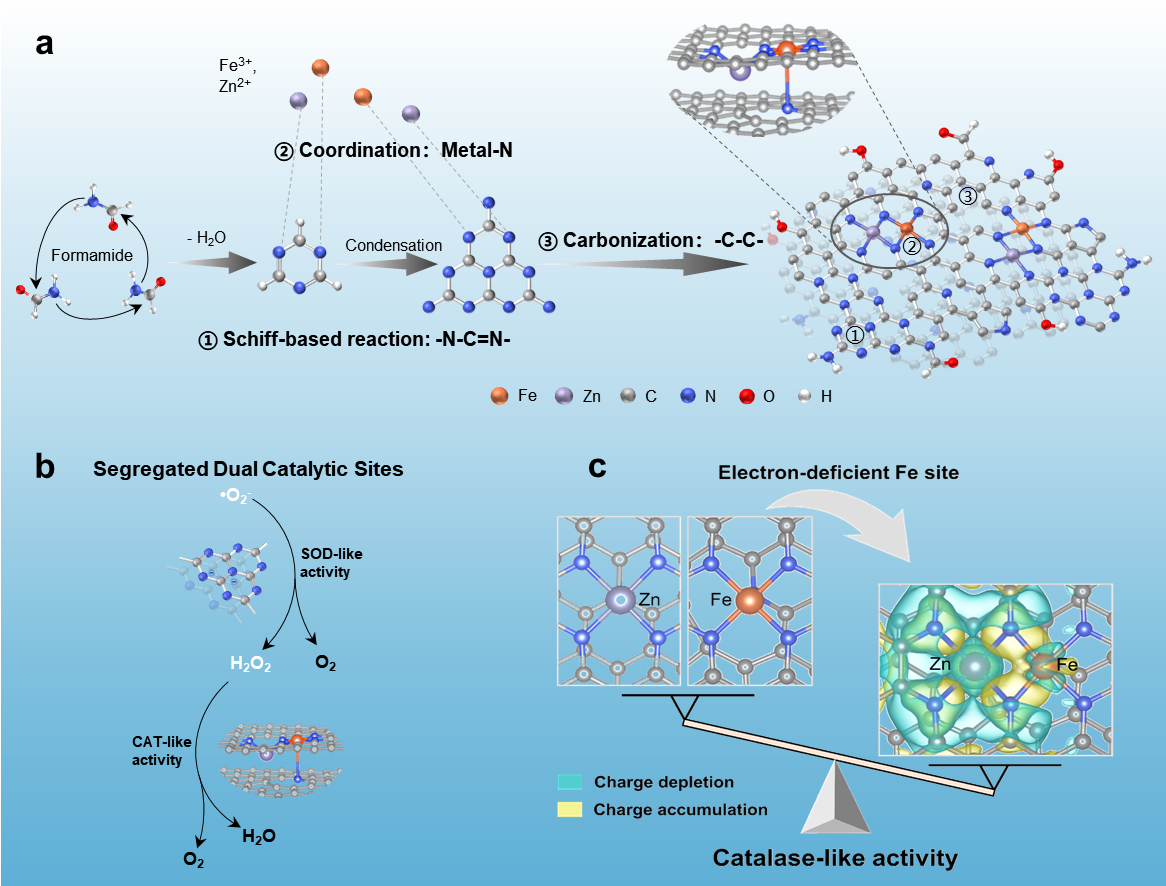
图5. FeZn-NC纳米酶的制备示意图(a)、双催化位点示意图(b)以及缺电子效应增强的CAT-like活性调控机制示意图(c)。


 沪公网安备 31010502006565号
沪公网安备 31010502006565号