近年来,一种可作为免疫药物递送平台的纳米工程化免疫生态位(niche)由于可重编程肿瘤微环境(TME)有望显著提高免疫治疗效果,引起了研究者广泛关注。由水凝胶材料构成的类生态位由于可长效滞留肿瘤区域,模拟或重建天然细胞外基质,有望成为理想的可定制的个体化治疗平台。
近期,中国科学院上海硅酸盐研究所陈航榕研究员课题组构建了一种酶介导的氧气响应成胶和活性氧(ROS)响应断键能力的壳聚糖水凝胶(CS-FTP-gel)。研究者在壳聚糖分子链上共轭接枝了氧气响应的阿魏酸(FA)片段和ROS响应的酮缩硫醇(TK)片段,同时连接抗血管生成抑制剂并负载乏氧前药,当所合成的功能化壳聚糖CS-FTP与漆酶混合注射入肿瘤时,CS-FTP可被漆酶催化并与氧气反应快速交联,在肿瘤组织周围原位形成三维网络水凝胶结构。同时这一耗氧过程进一步强化了肿瘤微环境的乏氧水平,从而激活前药发挥化疗作用。此外水凝胶ROS片段响应肿瘤区域高表达的双氧水促使分子链断裂,从而释放抗血管生成药物,有效抑制肿瘤新生血管生成,发挥饥饿疗法作用的同时抑制肿瘤转移。在活体动物水平上,研究者以氧气敏感的18FMISO作为探针,采用micro-PET成像技术证实CS-FTP-gel可有效强化肿瘤的乏氧水平,为乏氧化疗提供理想的微环境(图1)。活体实验进一步证实了该类生态位水凝胶递送平台对4T1乳腺癌原位瘤展示出良好的肿瘤生长抑制效果,抑制率达83.88%。
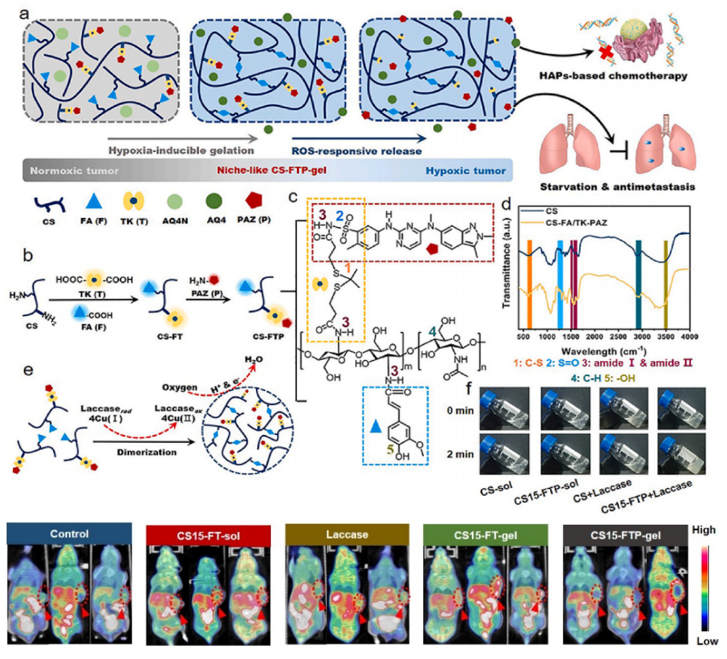
图1 基于壳聚糖的类生态位功能水凝胶构建策略与小动物模型乏氧增强影像表征
相关研究以In situ forming oxygen/ROS-responsive niche-like hydrogel enabling gelation-triggered chemotherapy and inhibition of metastasis为题发表在Bioactive Materials, 21(2023):86-96. 论文第一作者为上海硅酸盐所2015级硕博连读研究生陈世雄(已毕业),陈航榕研究员和复旦大学附属肿瘤医院核医学科宋少莉教授为该研究共同通讯作者。
近期该课题组进一步针对常规免疫检查点阻断疗法对低免疫原性的三阴乳腺癌临床治疗不敏感,响应率低等临床治疗难题,创新合成了一种具有内外源刺激响应功能的类生态位新型水凝胶。研究者将含有功能声敏剂TiOx@CaO2的TSPBA和装载免疫检查点抑制剂aPD-L1的PVA分别瘤内注射后,可在肿瘤组织周围原位快速形成三维网络凝胶结构。该有机无机复合水凝胶可响应肿瘤内源弱酸性和高表达H2O2,逐渐降解并释放免疫检查点抑制剂和无机声敏剂等活性组分,同时产生氧气缓解肿瘤缺氧环境,从而下调HIF-α表达,诱导巨噬细胞向M1型极化,有助于逆转肿瘤免疫抑制微环境(图2)。通过易转移型三阴乳腺癌模型活体实验证实了基于类生态位水凝胶递送免疫类药物可以实现在肿瘤区域长效滞留,有利于在外场超声刺激下实施多重协同的抗肿瘤治疗;进一步联合免疫检查点抑制剂aPD-L1,可有效激活T细胞免疫,显著增效抗肿瘤免疫疗效并有效抑制肺转移,为易转移型三阴性乳腺癌的高效治疗提供了一条新途径和材料支撑。
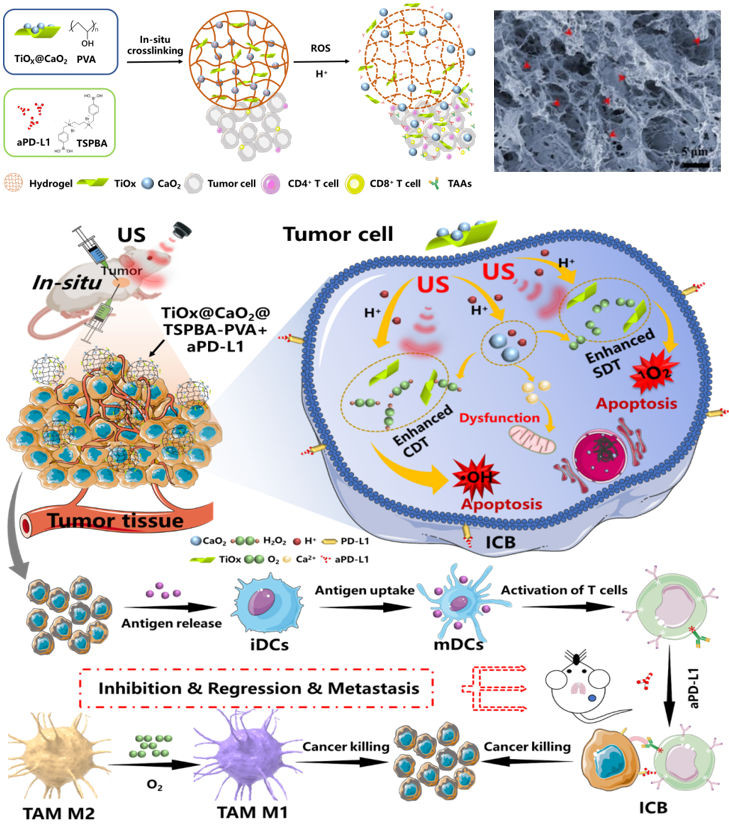
图2 响应型有机无机复合水凝胶的构建与超声介导的抗肿瘤免疫治疗示意图
相关研究以“In situ forming pH/ROS-responsive niche-like hydrogel for ultrasound-mediated multiple therapy in synergy with potentiating anti-tumor immunity”为题发表在Materials Today, DOI: org/10.1016/j.mattod.2023.03.025。该论文第一作者是上海硅酸盐所和中国科学院大学杭州高等研究院联合培养的2021级在读博士生代子登,上海硅酸盐所陈航榕研究员和李晓宏博士后为该论文共同通讯作者。
相关研究获国家自然科学基金重点项目(32030061)和上海市科委基础重点(19JC1415600,21JC1406000)等项目支持。
附原文链接:
https://www.sciencedirect.com/science/article/pii/S2452199X22003322?via%3Dihub
https://www.sciencedirect.com/science/article/pii/S1369702123000871?dgcid=author


 沪公网安备 31010502006565号
沪公网安备 31010502006565号