甲醇(CH3OH)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。传统的甲醇工业生产主要依赖费托合成过程,其反应条件较为苛刻(50-100 bar, 200-300 ℃),且造成了大量碳排放(生产每吨甲醇排放超过30 kg CO2)。为降低甲醇生产过程中的能耗和污染,迫切需要新的低碳技术。基于可再生电力驱动的电催化二氧化碳还原反应(CO2RR)是一种潜力巨大的可再生燃料生产技术,可在接近零碳排放的状态下将CO2转化为气态或液态燃料分子。目前,最常用的铜基催化剂可催化CO2RR生成多种一碳(C1)和多碳(C2+)的高附加值产物。然而,在水溶液中利用电化学CO2RR制备CH3OH的研究报道还相对较少,选择性和产率通常远低于气相的甲烷(CH4)产物(图1a)。
近日,中国科学院上海硅酸盐研究所黄富强研究员、王家成研究员和复旦大学郑耿锋教授开展合作,在电催化CO2转化CH3OH研究方面取得重要进展。基于现代软硬酸碱(HSAB)理论,他们发现Cu催化位点的电子云离域特性对CO2RR过程中的CH3OH选择性影响显著。
在该研究工作中,合作团队首先设计合成并解析了氰胺亚铜(Cu2NCN)化合物。晶体结构分析和理论计算结果表明,长链氰胺根 [NCN]2-的引入拉远了相邻的Cu原子的间距使其成为较为孤立的活性位点,在电催化CO2RR过程中,孤立的Cu(I)位点可抑制C-C偶联,从而减少C2+产物的生成(图2)。另一方面,在强配位 [NCN]2-阴离子的极化作用下,Cu(I)周围的电子云弥散明显,理论计算其导带底有效电子质量远低于金属Cu,呈现高度的离域态特征,即形成了更软的阳离子酸位点(图1c)。基于软硬酸碱理论,软的酸性位会削弱硬碱(*O、*OR,R = H或烷基)的键连强度。因此,这种Cu(I)的电子离域态削弱了Cu-O键强度,使得 Cu-*O-CH3的这一关键反应中间体更倾向于发生Cu-O键断裂,并最终加氢生成甲醇(图1b,图3和图5)。Cu2NCN电催化剂在水溶液中表现出优异的电催化合成CH3OH选择性与活性(图4)。原位拉曼测试也验证了反应过程中关键反应中间体的生成。
该研究针对水系电解液中电化学CO2还原制备CH3OH的选择性与活性较低这一挑战提出了新思路。利用氰胺亚铜催化剂上Cu位点的电子离域态的增强,调控了关键中间体的不同断键位点的相对强弱,实现高选择性的甲醇产物制备。
相关研究成果以“Delocalization State-Induced Selective Bond Breaking for Efficient Methanol Electrosynthesis from CO2”为题发表在Nature Catalysis上(2022,doi: 10.1038/s41929-022-00887-z)。上海硅酸盐所博士生孔舒仪和复旦大学博士生吕希蒙为论文共同第一作者。该研究工作得到科技部国家重点研发计划(2018YFA0209401)、国家自然科学基金(22025502, 21975051, 92163117, 52072389)等项目的资助和支持。
文章链接:https://doi.org/10.1038/s41929-022-00887-z

图1. Cu催化位点的电子云离域态对产物(甲烷或甲醇)的选择性影响示意图。
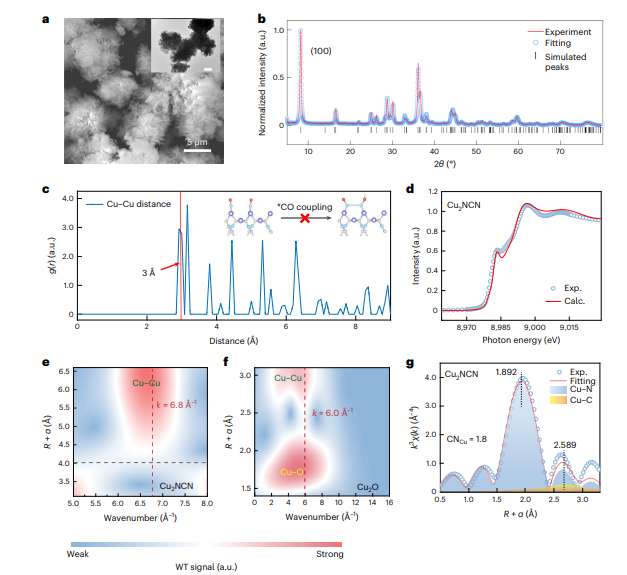
图2. Cu2NCN的形貌、XRD精修、Cu-Cu径向分布函数计算和同步辐射表征。
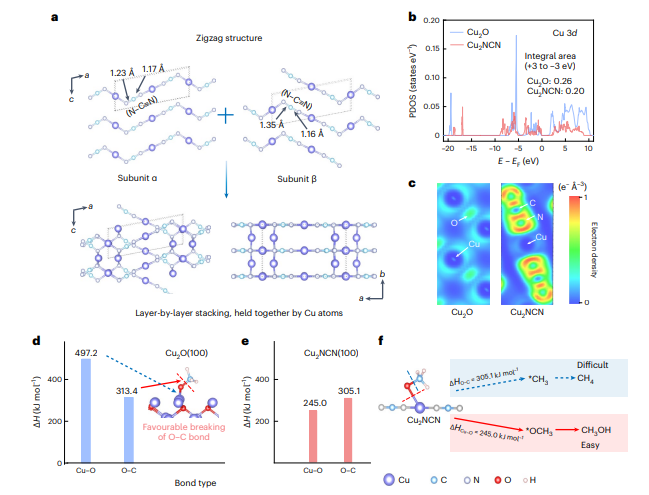
图3. Cu2NCN的晶体结构、离域性和关键中间体*OCH3的键解离焓计算。
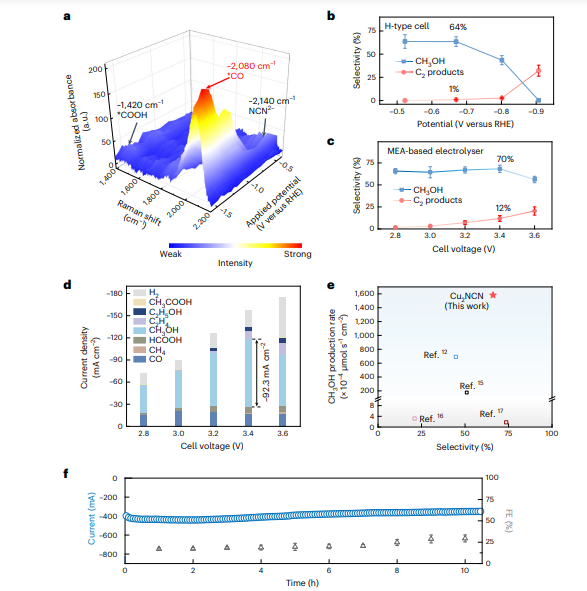
图4. Cu2NCN的电催化CO2RR性能
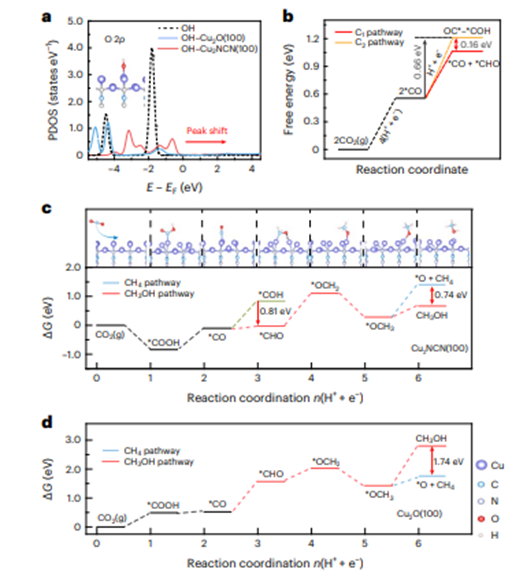
图5. 相关电催化CO2RR路径的理论计算


 沪公网安备 31010502006565号
沪公网安备 31010502006565号