
磁电催化纳米医学

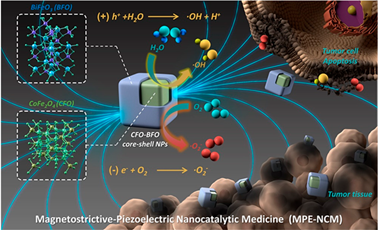
典型的ROS用于癌症治疗的方式包括:光动力疗法(PDT)、声动力疗法(SDT)、化学动力学疗法(CDT)、放射动力疗法(RDT)、电化学疗法(EchT)、电动疗法(EDT)和压电化学催化疗法(PCT)等。在这些治疗模式中,具有生物活性成分、高表面积和丰富晶格缺陷的各类功能纳米颗粒在肿瘤区域被用作纳米催化剂、反应物或反应底物,在光、超声、电离辐射、热和电流等外源性刺激或内源性肿瘤微环境(弱酸性、过量H2O2和乏氧),生成具有高细胞毒性的ROS。然而,在上述治疗模式之外,利用交变磁场(非侵入性、强度可控和无穿透深度限制的外界物理刺激)干预下的磁电响应过程产生ROS进行催化肿瘤治疗的研究尚未见报道。
为验证交变磁场诱导的微观应变和电场驱动的磁电催化效应,通过研究磁场处理的CFO-BFO NPs有机物降解曲线、电子顺磁共振特征峰以及静磁场条件下对单个核壳纳米颗粒的有限元模拟,我们发现CFO-BFO NP具备响应外界磁场发生磁致伸缩效应产生的电势分布和ROS生成性能(图1)。通过CCK-8定量了CFO-BFO NPs的磁电驱动ROS生成效率,发现在不同浓度CFO-BFO NPs共孵育24和48小时后,在高达500 μg mL-1的CFO-BFO浓度下,可以观察到细胞存活率得到基本保持,这表明磁电纳米颗粒具有良好的体外生物相容性。针对4T1癌细胞系评估了CFO-BFO NP磁电纳米催化疗法的体外细胞毒性,当磁场强度和处理时间增加时,产生的ROS逐渐增多,并导致细胞活力的降低。该CoFe2O4-BiFeO3在交变磁场的刺激下,能够在体内外催化水的氧化和氧分子的还原,分别产生羟基(·OH)和超氧自由基(·O2-)两种活性氧,从而诱导肿瘤细胞死亡和局部实体瘤消融。
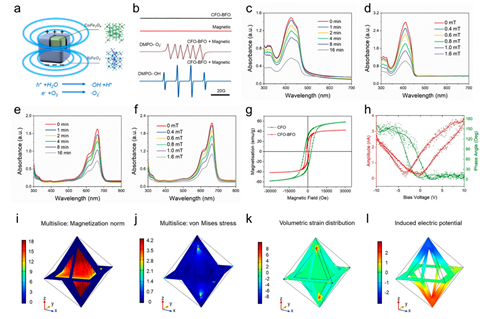
图1. 磁场作用下磁致伸缩-压电效应的机制探索
该研究工作以“Magnetostrictive-Piezoelectric-Triggered Nanocatalytic Tumor Therapy”为题发表在“Nano Letters”上(Nano Letters, 2021, 21, 6764?6772, DOI: 10.1021/acs.nanolett.1c01313)。第一作者为2018级博士生葛敏,通讯作者为施剑林院士和林翰副研究员。研究工作得到了国家自然科学基金项目、中国科学院基础前沿科学研究计划、中国科学院特别研究助理资助项目的资助和支持。

