
温和磁热激活固有免疫用于肝癌治疗

近年来,肿瘤的磁热疗法(MHT)因其良好的治疗效果、无创性和出色的组织穿透性受到人们越来越多的关注。但目前MHT的临床实验很少,而且都是通过瘤内滴注或局部注射将磁性材料注射到病灶部位,局部注射确实可以将磁性材料直接递送到体表的肿瘤内,但是对身体深处的肿瘤只能采用静脉注射的方式递送磁性材料。由于大部分肿瘤都在身体内部深处,所以研究者们认为,基于静脉注射磁性材料的MHT在肿瘤的治疗中有着重大的临床潜力。与皮肤下的浅表肿瘤不同,深层肿瘤嵌在器官和组织中。因此,用于肿瘤消融(> 50 ℃)的高温传统MHT会不可避免地对周围器官和组织造成不可逆的损伤,这意味着MHT的温度应保持在正常组织的热耐受范围内。据报道,正常组织在43 ℃左右只会受到轻微的影响,幸运的是,这个温度下的热疗可以治疗肿瘤。因此,温度在43 ℃左右的MHT(即温和磁热疗法)被认为是一种有效的肿瘤治疗模式,具有很好的临床应用潜力。然而,目前静脉注射磁热材料的MHT存在两个瓶颈问题:一是磁热材料的产热效率较低,二是静脉注射的磁热材料对病灶部位靶向效率不足。
针对第一个问题,研究者们通过改变磁热材料的尺寸、形貌、成分、磁各向异性常数等,来提高其磁热性能。然而,目前磁热性能最好的纳米颗粒不再具有超顺磁性,这意味着纳米颗粒会自发聚集,不适合应用于生物医学领域。施剑林院士组在之前的研究中合成了超顺磁性的核壳纳米颗粒,并将其用于皮下肿瘤的高效MHT,由于软硬磁之间的交换耦合作用,其产热效率相对较高。此外,研究者们还发现Zn2+的掺杂可以有效增强铁酸盐纳米颗粒的磁性,从而进一步提高磁热性能,并且尺寸的增大也会提升纳米颗粒的产热效率。
第二个问题,静脉注射的磁性纳米颗粒无法在病灶区域富集,这是由于大多数静脉注射的纳米颗粒会被困在单核吞噬细胞系统(MPS)中,这阻止了纳米颗粒在病灶区域的有效积累,成为其临床转化的一个重要障碍。根据目前的研究,大部分静脉注射后的超顺磁性纳米颗粒将分布在肝脏,因此,静脉注射磁性纳米材料的MHT在治疗肝脏疾病方面很有潜力,特别是肝癌,它是全球第六大常见癌症,也是癌症病人死亡的第四大原因。采用温和MHT治疗肝癌具有以下优势:第一,由于磁性纳米颗粒在肝脏的优先摄取,温和MHT治疗肝癌需要的纳米颗粒剂量要低得多;第二,温和MHT是一种物理治疗,其副作用比化疗和放疗要小得多;第三,肝脏中丰富的血管可以保证快速散热,从而降低热疗对肝脏组织的损伤。而且,肝脏极强的恢复和再生能力也会进一步降低温和磁热的副作用。此外,热疗具有激活免疫系统的潜力。研究表明,温和热疗在体外和体内都可以激活自然杀伤细胞(NK细胞)。鉴于NK细胞在肝脏淋巴细胞中占很大的比例且与患者的预后和生存呈正相关,温和MHT对肝癌的治疗作用可通过激活NK细胞相关免疫反应来增强。
基于以上背景,我们团队首次利用静脉注射的纳米材料会优先被肝脏摄取的不利条件,使磁热纳米颗粒被动富集于肝脏,产生温和磁热治疗肝脏原位肿瘤。如示意图1所示,我们在前期基础上合成了一种核壳结构的、Zn2+掺杂的Zn-CoFe2O4@Zn-MnFe2O4超顺磁性纳米颗粒(ZCMF),由于软硬磁之间的交换耦合作用、Zn2+的掺杂和尺寸的增大,表现出优异的、高度可控的磁热性能。为进一步提高ZCMF对HepG2细胞(人肝癌细胞)的靶向作用,减少对正常组织的损伤,用血管内皮生长因子(VEGF)抗体修饰ZCMF,该抗体能特异性地与HepG2细胞上过表达的VEGF结合。
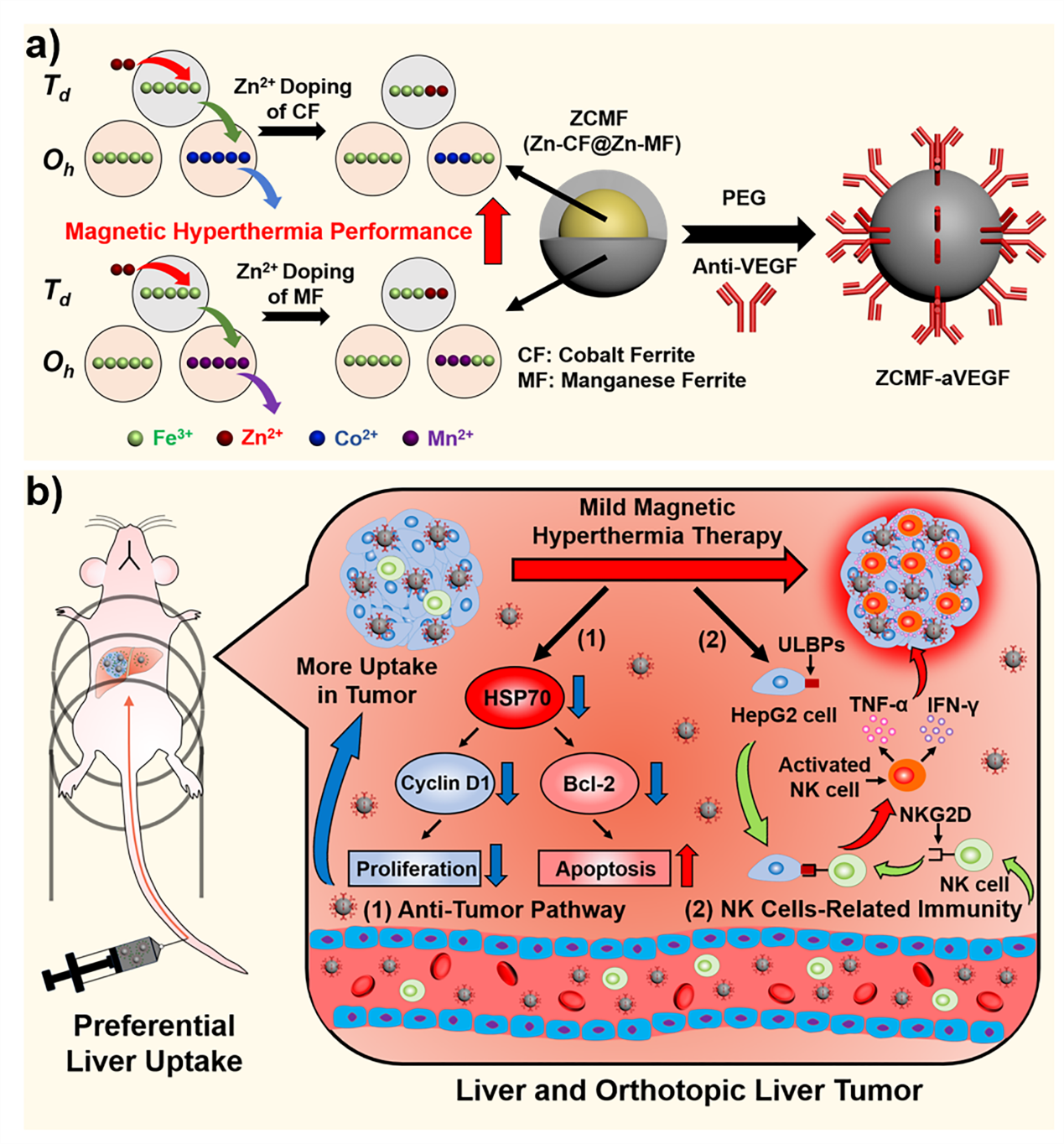
Scheme 1. 磁热纳米材料磁性增强的原理图和温和磁热治疗及其诱导的抗肿瘤固有免疫反应用于治疗原位肝癌的示意图。(a)ZCMF通过Zn2+掺杂和核壳结构增强磁性的原理图以及之后通过VEGF抗体的表面修饰形成ZCMF- aVEGF的示意图。(b)温和MHT通过抑制肿瘤细胞的增殖以及诱导产生NK细胞相关抗肿瘤免疫反应以治疗原位肝癌的示意图。
结果发现,基于ZCMF的温度为43 ~ 44 ℃的温和MHT几乎完全抑制了肝癌细胞的增殖和肿瘤的生长,这与抑制热休克蛋白70(HSP70)的表达有关。更重要的是,温和MHT治疗后的肝癌细胞能够通过显著上调多种UL16结合蛋白(ULBPs)的表达来激活NK细胞,因为ULBPs是NK细胞的自然杀伤细胞2族成员D受体(NKG2D)的配体。最后,在温和MHT的治疗及其诱导的NK细胞相关固有免疫反应的作用下,皮下异种移植瘤和肝脏原位肿瘤的生长几乎完全被抑制,如图1所示。
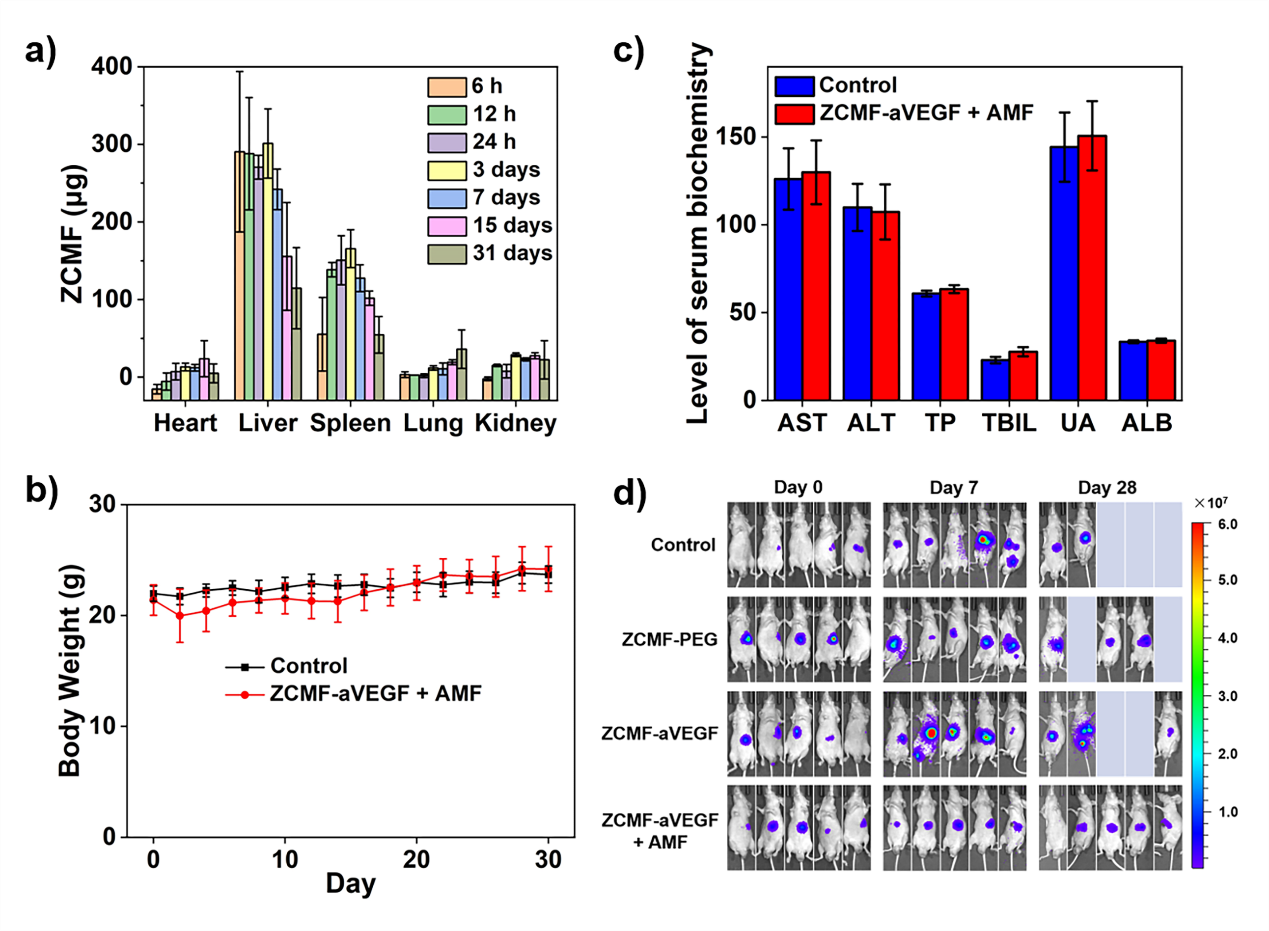
Figure 1. 温和MHT治疗肝脏原位肿瘤的体内生物安全性和有效性。
结论: 通过软硬磁的交换耦合作用、掺杂Zn2+和尺寸调节等方法,合成了一种具有优异、可控的磁热性能的核壳结构磁性纳米颗粒(ZCMF)。在ZCMF上修饰VEGF抗体增强了HepG2细胞摄取ZCMF-aVEGF的效率和选择性。基于ZCMF-aVEGF的温和MHT对HepG2细胞具有出色的治疗效果,其原因是抑制了HSP70的表达,进而抑制了Cyclin D1和Bcl-2的表达。值得注意的是,温和MHT可以显著上调HepG2细胞中ULBPs的表达,表明温和MHT治疗后的HepG2细胞可以激活NK细胞。更重要的是,ZCMF-aVEGF在瘤内富集后,温和MHT可以完全抑制小鼠的HepG2皮下瘤和原位肝脏肿瘤的生长。此外,由于激活了NK细胞相关的固有免疫反应,即使在降低温和MHT治疗频率的情况下,疗效仍可持续,从而延长了小鼠的生存时间。因此,温和MHT作为一种安全的癌症治疗策略,在未来的肝癌临床治疗中具有广阔的应用前景。
全文链接:

